肠道菌群 - Nature
原文链接:肠道微生物如何影响大脑?
最开始接触这一概念是我就像文章开头所说一样,抱有深深的怀疑,尤其是加上电视上的乳酸菌广告。现在看来只是与石墨烯、纳米材料等一样被伪科学借用了名字。肠道菌群是一门还在发展完善、不适宜面向大众的学科。我已经可以想象,未来越来越多的保健品会主打肠道菌群的概念…
2006年,神经科学家Jane Foster刚成立自己的实验室后不久,就发现了一些她觉得肯定会让这个领域沸腾的东西。当时,她和她的团队正在研究两组小鼠:一组小鼠的肠道中有多种健康的微生物,另一组缺乏微生物群。他们注意到,没有肠道细菌的小鼠似乎不像健康小鼠那么焦虑。当被放置到一个迷宫里,有些路径是开放的,有些路径有墙围着,它们更偏好暴露在外的路径。肠道中的细菌似乎在影响它们的大脑和行为。
来自加拿大麦克马斯特大学的Foster把这项研究写成论文,并投稿发表,结果被拒。她重写后再投,还是被拒。“大家都不信。他们认为那是一个假象。”她说。最后,经过三年七次投稿,她终于获得了一封接收信[1]。
John Cryan 是爱尔兰科克大学的一名神经科学家,他和Foster几乎同一时期加入这个领域,完全了解她的感受。谈到肠道细菌和大脑之间的联系时,“我感到热切地想要‘传道’。”他说。他回忆起2014年参加的一场阿尔茨海默病会议。“我从没经历过比那更受冷遇的演讲。”
然而,如今肠脑轴已成为主要神经科学会议的一个特色,Cryan说他不再是“那个爱尔兰来的疯子”。在过去的十年里,成千上万的出版物显示,肠道中数以万亿计的细菌可能对大脑产生深远的影响,并且可能与一系列疾病有关。美国国立卫生研究院等资助机构正在投资数百万美元来探索这种联系。
但随着这种兴趣的激增,也产生了大肆炒作。澳大利亚悉尼大学研究微生物组研究领域的哲学家Maureen O’Malley说,当许多研究只显示了相关性时,一些肠脑研究人员却声称或暗示了因果关系,“你是真的找到了一个原因,还是不过又发现了一种效应?”
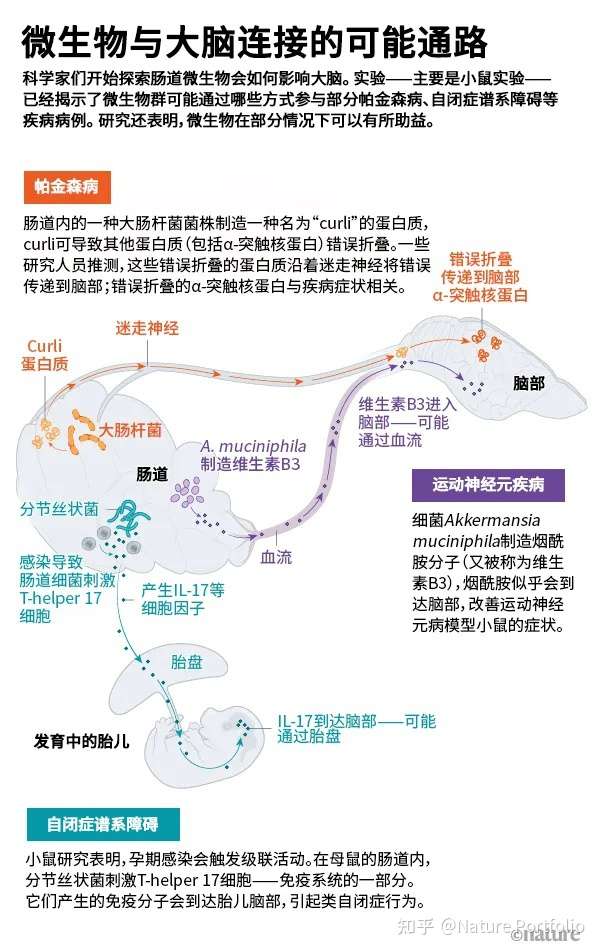
不过,O’Malley说,近年来,该领域取得了长足的进步。一些研究小组不仅仅将微生物群作为整体来讨论,而是开始深入研究,识别特定的微生物,绘制出将微生物与大脑相连的复杂甚至惊人的通路。“这么做才允许作出因果归因。”她说。小鼠研究——以及基于人类的初步研究——表明微生物可以触发或改变帕金森病、自闭症谱系障碍等疾病的进程(见“微生物与大脑连接的可能通路”)。旨在调整微生物群的疗法也许可以帮助预防或治疗这些疾病,一些研究人员和公司已经在开展人体临床试验,检验这一观点。
加州理工学院的微生物学家Sarkis Mazmanian说,现在还处于初期阶段,但用于治疗一些难治脑部疾病的新疗法展现出了令人振奋的前景,特别是考虑到操纵肠道比操纵大脑容易多了。他说,直指脑部的疗法一直是一个挑战,“但你肯定能改变微生物群。”
信号传输
1817年,英国外科医生詹姆斯·帕金森(James Parkinson)描述了一些后来被称为帕金森病的“颤抖麻痹”病例。有一个人的双臂出现麻木和刺痛感。帕金森注意到,该男子的腹部似乎含有“相当大的堆积物”。他让那人服用泻药,十天后他的肠道排空,症状消失了。
帕金森可能已经发现了问题。一些患这种疾病的人早在出现行动障碍之前就患有便秘。许多研究人员已经接受了这种疾病源自肠道的观点,至少在某些情况下是这样。
要理解这个观点,有必要先稍稍了解一下这种疾病。帕金森病的标志性症状——颤抖、僵硬和行动缓慢——随着负责协调运动的神经元开始死亡而出现。这些神经元为什么会死亡,原因至今不甚明确,但α-突触核蛋白似乎起着关键作用。在帕金森病患者中,该蛋白质错误折叠。第一个错误折叠的蛋白质会导致更多的错误折叠,直到被称为路易体(Lewy bodies)的有害团块开始在脑部形成。
是什么触发了这种级联反应?2015年,美国易斯维尔大学的神经科学家Robert Friedland提出了一个新理论。他读到说,肠道细菌可以产生与错误折叠α-突触核蛋白结构相似的蛋白质,因此他假设细菌蛋白可能为错误折叠[2]提供了模板。他和他的同事给小鼠喂食一种特殊的大肠杆菌菌株,这种大肠杆菌会在肠道中产生一种叫做“curli”的团块蛋白质;他们发现,小鼠脑部的α-突触核蛋白积累增多[3]。Mazmanian及其团队去年发表的成果支持Friedland的理论[4]。
目前还不清楚肠道中的信号是如何到达大脑的,但一个可能的通道是迷走神经。迷走神经将脑干与许多器官(包括结肠)连接起来,是在大脑和身体其他部位之间传递信号的十二个颅神经中最长的。“它真的是一条高速公路。”Cryan说。基于人类和动物的研究表明,迷走神经至少在肠道和大脑之间传递某些信息方面起着至关重要的作用。
20世纪70年代,胃溃疡的一种常见疗法是切除所有或部分神经,以抑制胃酸的产生。但近几十年来,研究人员注意到了一个奇怪的副作用:接受过这种手术的人似乎不太容易受到帕金森病的影响[5]。
在一项小鼠研究中,将错误折叠的α-突触核蛋白注射进小鼠肠道后,它又在大脑中出现了。但是,如果研究人员先切除了迷走神经,则没有α-突触核蛋白出现在大脑中[6]。注射的α-突触核蛋白本身似乎留在肠道中,但约翰斯·霍普金斯大学的神经科学家、研究的共同作者Valina Dawson认为,可能存在多米诺骨牌效应:错误折叠的蛋白将错误传给迷走神经,直到大脑中的蛋白质最终发生错误折叠。Mazmanian及同事目前正在开展实验,看看在迷走神经被切除的小鼠身上,肠道中的curli蛋白是否仍然能引起帕金森病症状。
由于错误折叠的蛋白是影响大脑的几种其他疾病的标志,这些疾病包括阿尔茨海默病和运动神经元病(肌萎缩侧索硬化,或ALS),Friedland说细菌蛋白也可能与这些疾病有关。Dawson认为这个想法有道理,但说细菌淀粉样蛋白并不是唯一需要考虑的因素。例如,帕金森病是一种复杂的疾病,在不同的人中有不同的表现。不过,她说,“这可能是开启第一步的方式。”
加速恶化
肠脑连接的支持者说,微生物群能做到的不仅仅是触发一些神经退行性疾病:它也可能影响其严重程度。Eran Elinav是以色列魏茨曼科学研究所和海德堡德国癌症研究中心的免疫学家,他对ALS的进展差异感到震惊:一些ALS患者进展缓慢,而另一些则迅速恶化。Elinav想知道微生物群是否有助于解释这些差异,因此他和他的团队开始使用最常见的一种ALS小鼠模型。他们使用抗生素消除了微生物群、或出生时就缺乏微生物群的小鼠时,发现这类小鼠的ALS进展比拥有正常微生物群的小鼠快得多[7]。
研究小组比较了ALS小鼠及其同窝健康小鼠的肠道细菌,发现了几种似乎与该疾病有关的微生物物种。他们煞费苦心地将这些物种一一移植到另一组没有任何肠道细菌的小鼠体内,鉴定出了两个使ALS症状恶化的微生物物种,以及另一个似乎使症状好转的物种。“然后我们问自己,‘这种只生活在肠道中的菌株,怎么会如此神奇地影响到一种集中于脑的疾病?’”Elinav说。
罪魁祸首可能是细菌代谢物——由细菌产生的小分子,它们可以进入血流,在全身运行。Elinav说,血液中至少有一半的小分子是“由微生物制造或由微生物调节的”。他和他的团队分析了有益微生物产生的代谢物,并给容易患上ALS的小鼠注射了一种叫做烟酰胺(也被称为维生素B3)的分子。他们发现烟酰胺进入了脑部,并改善了小鼠的症状[7:1]。“我们可以证明有一种细菌,我们可以证明有这种细菌的产物,我们可以证明它‘游’到正确的目标器官,并做一些有利于病程的事情。”他说。
他们比较了ALS患者及其未受影响的家庭成员的微生物群,发现ALS患者体内的烟酰胺较少[7:2]。该代谢物可以作为一种补充剂,Elinav说,他和他的同事正计划针对它开展一项临床试验。
至少有一组已经在一个小型试验中测试了维生素B3作为ALS的治疗方法,不过试验中也结合使用了其他化合物。他们在四个月的时间里,向ALS被试注射维生素B3。治疗组的人有所改善,但安慰剂组几乎所有人的健康状况都下降了[8]。
“这才刚刚开始。”Elinav说。还有更多的细菌和代谢物存在,机体内的每一个细胞都会受到它们的影响。一旦你意识到这一点,他说,“你开始明白,微生物群的影响可以大大扩展到它们实际生存的地方之外。”
代际效应
这种影响甚至可能代代相传。以自闭症谱系障碍(ASD)为例,该病病因尚不清楚,但根据流行病学研究,母亲在怀孕期间的感染似乎增加了孩子患ASD的风险。例如,在瑞典的一个包含近180万人的队列中,母亲曾在怀孕期间因感染而住院的,出生婴儿以后被诊断为ASD的风险要高79%[9]。
小鼠研究也支持这种联系。为了模仿感染,研究人员给怀孕的小鼠注射双链RNA,小鼠身体将其视为病毒入侵。相较于那些未受注射小鼠的后代,前一种小鼠的后代表现出更多的重复行为和焦虑,并且与其他小鼠的互动更少——这些症状映射了ASD患者的症状[10]。
麻省理工学院皮考尔学习与记忆研究所的神经科学家Gloria Choi和她的丈夫兼合作者、波士顿哈佛医学院免疫学家Jun Huh想知道原因。他们聚焦的这类细胞通过产生一种被称为细胞因子的分子来抵御细菌和真菌。Choi和Huh使用小鼠模拟感染,发现辅助性T细胞17(Th17)变得过度活跃,产生一种叫做IL-17的细胞因子。这种分子进入了发育中的小鼠的脑部——可能通过胎盘,然后与大脑受体结合。这似乎对小鼠产生了深刻的影响:研究人员发现,成年后代的神经活动增加了,导致它们出现自闭症样行为[11]。
但是,“并不是每个在怀孕期间被感染或住院的孕妇都必然会生下患有神经发育障碍或自闭症的孩子。”Huh说。一定有什么东西使母亲的免疫系统转向这种过度活跃的状态。Choi和Huh专注于一组长而细的肠道微生物——分节丝状菌,这种微生物此前被证明能够促进Th17细胞的形成。他们对怀孕小鼠使用抗生素,以杀死这些细菌,然后刺激免疫反应,发现幼崽没有任何行为差异[12]。
Choi和Huh渴望了解新冠病毒大流行是否会导致患自闭症的风险增加,他们正在收集感染SARS-CoV-2的孕妇的样本,并编录其肠道中的细菌和血液中的IL-17水平。加州大学戴维斯分校研究自闭症的David Amaral说,鉴于新冠病毒像任何其他感染一样,会激活母体的免疫系统,因此SARS-CoV-2可能会增加大脑发育发生改变和患上潜在精神疾病的风险。研究人员尚未找到支持这一理论的证据。
休斯顿贝勒医学院的神经生物学家Mauro Costa-Mattioli也在研究细菌与自闭症之间的关系。但是,他没有发现导致这种疾病的微生物,而是发现了一种可能改善其症状的微生物。
大约五年前,Costa-Mattioli偶然发现了这种细菌。当时,他正在研究后代具有类似自闭症症状的小鼠。当这些小鼠和典型发育小鼠被安置在一起(并且像所有小鼠都会做的那样,吃后者的排泄物),它们的自闭症样行为消失了。Costa-Mattioli和他的同事们发现,受影响的小鼠缺少一种特殊的细菌:罗伊氏乳杆菌。
他们在其他若干模型小鼠中测试了罗伊氏乳杆菌,这种细菌能够逆转每个模型小鼠的某些自闭症样行为。而且,就像帕金森病的研究一样,如果研究人员切断了迷走神经[13],就可以在小鼠中阻断这种作用。
罗伊氏乳杆菌究竟发送了什么类型的信号还不得而知。研究小组发现,有些罗伊氏乳杆菌菌株可以逆转自闭症样行为,而另一些则不能,研究人员现在正在努力鉴定其中涉及哪些基因。Costa-Mattioli说,如果他们能发现产生关键代谢物的基因,“我们可以把它放进任何细菌,那样我们可能就拥有潜在的治疗方法了。”这一策略尚未获得验证。
意大利的一个团队已经在尝试使用罗伊氏乳杆菌治疗80名自闭症儿童。被试将摄入罗伊氏乳杆菌或安慰剂片剂6个月,并被监测症状。Costa-Mattioli希望很快启动自己的试验。
它是否有效还有待观察,但都柏林三一学院的神经遗传学家Kevin Mitchell认为小鼠研究还不具有说服力。他说,考虑到这类疾病的复杂性,他认为关于治疗潜力的讨论为时尚早,而且“有点不负责任”。
与此同时,研究人员正在探索更多的脑部疾病,包括阿尔茨海默病和抑郁症。肠道微生物甚至可能影响大脑在受伤后如何恢复。德国慕尼黑路德维希·马克西米利安大学中风和痴呆症研究所的神经生物学家Corinne Benakis及其同事使用抗生素治疗小鼠,在诱发中风之前消除一些肠道细菌。他们发现抗生素可以降低脑损伤的严重程度[14]。
在这每一种疾病中,仍然存在许多机制问题。该领域的研究人员承认,他们还没有充分描述从微生物到大脑的通路。最棘手的一步将是在人类身上验证这些动物研究发现,并进入试验阶段。“这些都是非同寻常的观点,需要特别的证据。”Mitchell说。
但是人们非常感兴趣——不只是学术界。2019年2月,马萨诸塞州沃尔瑟姆市的Axial Therapeutics公司筹集了2500万美元的资金;该公司由Mazmanian联合创立,旨在开发神经退行性疾病和神经精神病疗法。另一家公司,位于马萨诸塞州萨默维尔市的Finch Therapeutics,正在开发一种用于自闭症的口服微生物药物;公司于2020年9月宣布,已经筹集了9000万美元。
在Cryan那次发表该主题的演讲遇冷以后,他目睹着数据越积越多。他发现越来越多的证据令人信服,并看到了基于微生物群疗法的巨大前景。“这不像你的基因组,除了怪怪父母和祖父母也没什么可做的。但你的微生物群是有可能改变的。这赋予患者极大的能动性,”他说,“真的很令人兴奋。”
参考文献:
Neufeld, K. M., Kang, N., Bienenstock, J. & Foster, J. A. Neurogastroenterol. Motil. 23, 255–e119 (2011). ↩︎
Friedland, R. P. J. Alzheimer’s Dis. 45, 349–362 (2015). ↩︎
Chen, S. G. et al. Sci. Rep. 6, 34477 (2016). ↩︎
Sampson, T. R. et al. eLife 9, e53111 (2020). ↩︎
Svensson, E. et al. Ann. Neurol. 78, 522–529 (2015). ↩︎
Kim, S. et al. Neuron 103, 627–641 (2019). ↩︎
de la Rubia, J. E. et al. Amyotroph. Lateral Scler. Frontotemp. Degen. 20, 115–122 (2019). ↩︎
al-Haddad, B. J. S. et al. JAMA Psychiatry 76, 594–602 (2019). ↩︎
Careaga, M., Murai, T. & Bauman, M. D. Biol. Psychiatry 81, 391–401 (2017). ↩︎
Yim, Y. S. et al. Nature 549, 482–487 (2017). ↩︎
Kim, S. et al. Nature 549, 528–532 (2017). ↩︎
Sgritta, M. et al. Neuron 101, 246–259 (2019). ↩︎
Benakis, C. et al. Nature Med. 22, 516–523 (2016). ↩︎